URL: https://www.desy.de/aktuelles/news_suche/index_ger.html
Breadcrumb Navigation
DESY News: Forscherteam findet neuen Ansatz für Mittel gegen Schlafkrankheit
News-Suche
Meldungen vom Forschungszentrum DESY
Forscherteam findet neuen Ansatz für Mittel gegen Schlafkrankheit
Mit ultrahellen Röntgenblitzen hat ein Forscherteam einen möglichen Angriffspunkt für neue Medikamente gegen die Schlafkrankheit aufgespürt: Die Wissenschaftlerinnen und Wissenschaftler haben die detaillierte räumliche Struktur eines lebenswichtigen Enzyms des Erregers entschlüsselt. Das Ergebnis liefert Hinweise auf einen möglichen Bauplan für einen Wirkstoff, der dieses Enzym gezielt blockiert und den Erreger somit absterben lässt, wie das Team um Christian Betzel von der Universität Hamburg, Lars Redecke von der Universität Lübeck und von DESY sowie Henry Chapman von DESY im Fachblatt „Nature Communications“ berichtet.
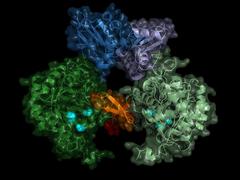
Struktur der IMP-Dehydrogenase des Parasiten: Das Enzyme bildet im aktiven Zustand Paare (Dimere), der Schalter des Enzyms (die Bateman-Region) ist in Blautönen dargestellt. Bild: Universität Lübeck/DESY, Lars Redecke
Auf der Suche nach einem möglichen Ansatzpunkt für Medikamente gegen den Erreger hatten die Forscherinnen und Forscher ein zentrales Enzym des Einzellers ins Visier genommen, die sogenannte Inosin-5'-Monophosphat-Dehydrogenase (IMPDH). „Dieses Enzym gehört zum zentralen Inventar jedes Organismus und ist ein interessantes Ziel für Medikamente, weil es den Haushalt zweier lebenswichtiger Nukleotide in der Zelle regelt: Guanosindiphosphat und Guanosintriphosphat“, sagt Redecke. „Die Zelle braucht diese Nukleotide zur Energieversorgung und zum Aufbau größerer Strukturen wie dem Erbgut. Wenn man diesen Zyklus unterbricht, stirbt die Zelle.“
Dieser Weg ist oft kompliziert, denn die meisten Biomoleküle lassen sich nur schwer kristallisieren. Gelingt die Zucht solcher Kristalle, sind sie gegenüber der energiereichen Röntgenstrahlung meist sehr empfindlich und werden schnell zerstört. „Es sind zwar bereits die Strukturen zahlreicher IMP-Dehydrogenasen bekannt, bei jener des Parasiten Trypanosoma brucei war die Kristallzucht bislang jedoch nicht erfolgreich“, berichtet Betzel, der auch im Exzellenzcluster CUI: Advanced Imaging of Matter von Universität Hamburg und DESY forscht.
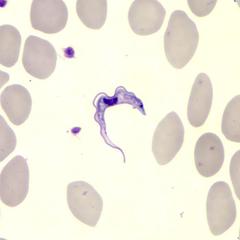
Das Team wählte daher einen alternativen Weg: Die Gruppe von Ko-Autor Michael Duszenko an der Universität Tübingen hat bestimmte Insektenzellen dazu gebracht, Biomoleküle in ihrem Inneren zu kristallisieren. Mit Hilfe dieser sogenannten In-cellulo-Kristallisation hatte dasselbe Team bereits ein anderes Enzym des Schlafkrankheit-Erregers entschlüsselt, Cathepsin B, das ebenfalls einen potenziellen Angriffspunkt für Medikamente darstellt. Tatsächlich produzierten die veränderten Insektenzellen auch Kristalle der nun untersuchten Dehydrogenase. Diese winzigen, nadelförmigen Kristalle wurden rund 5 tausendstel Millimeter (Mikrometer) dick und bis zu 70 Mikrometer lang, so dass sie aus den produzierenden Zellen herausstachen.
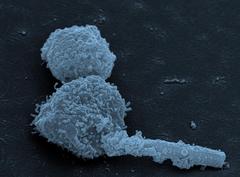
Die Mikrokristalle werden so lang, dass sie aus den Insektenzellen herausstechen. Bild: Universität Tübingen, M. Duszenko, und Universität Hamburg, C. Mudogo
Das Team zeichnete die Streubilder von mehr als 22 000 Mikrokristallen auf und konnte daraus die räumliche Struktur des Enzyms mit einer Genauigkeit von 0,28 millionstel Millimeter (Nanometer) genau berechnen – das entspricht in etwa dem Durchmesser eines Aluminium-Atoms. „Das Ergebnis zeigt nicht nur die genaue Struktur des Enzym-Schalters, der Bateman-Region, sondern auch, mit welchen Molekülen die Zelle das Enzym schaltet und wie diese sogenannten Ko-Faktoren an dem Enzymschalter andocken“, berichtet Karol Nass von DESY, der an dieser Studie im Rahmen seiner Doktorarbeit gearbeitet hat. Nass forscht heute am Paul-Scherrer-Institut in der Schweiz und ist zusammen mit Redecke Hauptautor der Veröffentlichung.

Eine Herausforderung bleibt dabei jedoch noch, den Dehydrogenase-Blocker so spezifisch zu konstruieren, dass er das Parasiten-Enzym blockiert, aber nicht das menscheneigene. Wenn dies gelingt, könnte die Methode möglicherweise auch auf andere Erreger ausgedehnt werden, erläutert Betzel. „Andere Parasiten haben einen sehr ähnlichen Aufbau, eventuell ließen sich auch die über die jeweilige IMP-Dehydrogenase angreifen. Das Enzym ist ein sehr interessantes Ziel für Medikamente, etwa auch gegen den Fuchsbandwurm oder den Erreger der Elephantiasis.“
An der Untersuchung waren die Universitäten Hamburg, Lübeck und Tübingen, die russische Akademie der Wissenschaften, die Arizona State University, das Lawrence Livermore National Laboratory in den USA, das Max-Planck-Institut für medizinische Forschung, das US-Forschungszentrum SLAC, die Universität Göteborg und DESY beteiligt.
Originalarbeit:
In cellulo crystallization of Trypanosoma brucei IMP dehydrogenase enables the identification of genuine co-factors; Karol Nass, Lars Redecke et al.; „Nature Communications“, 2020; DOI: 10.1038/s41467-020-14484-w